Manajemen Antibiotik pada Kaki Diabetik dengan Gangren: Sebuah Tinjauan Klinis Berbasis Bukti Berdasarkan Pedoman IWGDF/IDSA 2023
29 Jan 2026 • bedah
Deskripsi
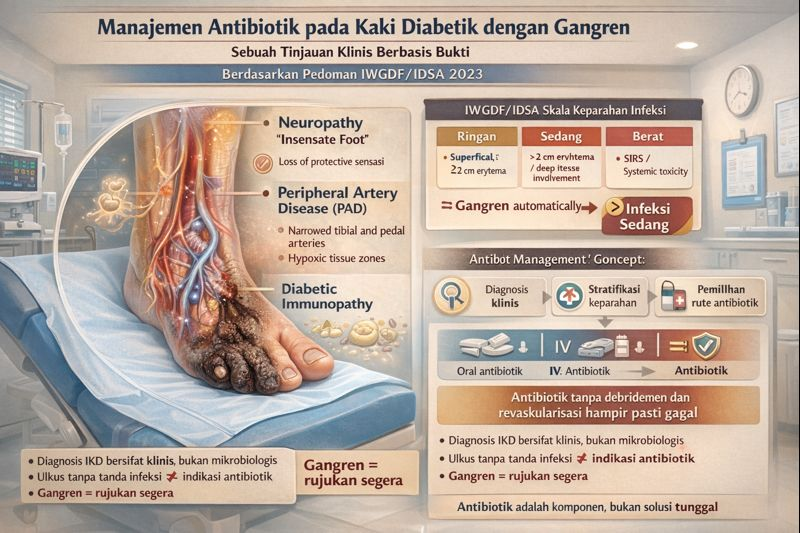
Bagian 1: Rangkaian Peristiwa Patofisiologis Gangren Kaki Diabetik
Gangren pada kaki diabetik bukanlah sekadar infeksi lokal, melainkan titik akhir katastropik dari suatu proses penyakit sistemik yang kompleks. Kondisi ini merupakan manifestasi kegagalan total mekanisme pertahanan dan perbaikan jaringan pada ekstremitas bawah, yang didorong oleh tiga pilar patofisiologis yang saling memperkuat: neuropati, penyakit arteri perifer (Peripheral Artery Disease - PAD), dan gangguan respons imun (imunopati).
Pemahaman mendalam terhadap interaksi sinergis dari triad ini adalah fundamental untuk manajemen yang rasional, yang menekankan bahwa terapi antibiotik hanyalah satu komponen dari strategi intervensi yang jauh lebih luas.
1.1. Fondasi Neuropati: Kaki yang Mati Rasa (The Insensate Foot)
Neuropati diabetik adalah komplikasi yang paling umum dan merupakan faktor risiko utama yang mengawali jalur menuju ulserasi dan gangren. Hiperglikemia kronis menginduksi kerusakan saraf melalui berbagai mekanisme, termasuk jalur poliol, akumulasi produk akhir glikasi lanjut (Advanced Glycation End-products - AGEs), dan stres oksidatif. Kerusakan ini bermanifestasi dalam tiga domain fungsional yang berbeda:
Neuropati Sensorik: Ini adalah komponen yang paling berbahaya, menyebabkan hilangnya sensasi protektif (Loss of Protective Sensation - LOPS). Pasien tidak lagi merasakan nyeri, tekanan, atau suhu secara normal. Akibatnya, trauma berulang—seperti tekanan dari sepatu yang tidak pas, menginjak benda tajam, atau luka kecil—tidak disadari dan tidak ditangani, sehingga memicu kerusakan jaringan awal yang menjadi cikal bakal ulkus. Kaki yang mati rasa ini menjadi rentan terhadap cedera yang tidak terdeteksi.
Neuropati Motorik: Disfungsi saraf motorik menyebabkan atrofi otot-otot intrinsik kaki. Hal ini mengganggu keseimbangan antara otot fleksor dan ekstensor, yang mengakibatkan deformitas kaki seperti hammer toes, claw toes, dan prominence kepala metatarsal. Deformitas ini menciptakan titik-titik tumpuan abnormal dengan tekanan plantar yang sangat tinggi, yang secara signifikan meningkatkan risiko kerusakan kulit dan ulserasi di area tersebut.
Neuropati Autonom: Kerusakan pada sistem saraf otonom mengganggu fungsi kelenjar keringat dan minyak, menyebabkan kulit menjadi sangat kering, pecah-pecah, dan rentan terhadap fisura. Retakan pada kulit ini menjadi gerbang masuk yang ideal bagi bakteri. Selain itu, neuropati autonom menyebabkan
shunting arteriovenosa, di mana darah dialirkan langsung dari arteriol ke venula, melewati jejaring kapiler. Fenomena ini secara paradoks mengurangi perfusi nutrisi di tingkat kapiler meskipun aliran darah total ke kaki mungkin meningkat, sehingga semakin menghambat penyembuhan.
1.2. Komponen Iskemik: Lingkungan yang Tidak Mendukung Penyembuhan
Penyakit arteri perifer (PAD) secara dramatis mempercepat progresi ulkus menjadi gangren dengan menciptakan lingkungan jaringan yang hipoksik dan kekurangan nutrisi. Diabetes tidak hanya meningkatkan prevalensi PAD tetapi juga mengubah karakteristiknya.
Penyakit Makrovaskular: Aterosklerosis pada pasien diabetes sering kali lebih difus, lebih distal (mengenai arteri tibialis dan peroneus di bawah lutut), dan bilateral. Lokasi yang distal ini membuat prosedur revaskularisasi menjadi lebih sulit secara teknis. Iskemia yang diakibatkannya secara langsung menghambat penyembuhan luka dengan membatasi pasokan oksigen dan nutrisi esensial ke jaringan. Lebih penting lagi, aliran darah yang buruk juga menghalangi pengiriman antibiotik sistemik dalam konsentrasi yang cukup ke lokasi infeksi, sehingga membuat terapi farmakologis menjadi tidak efektif.
Penyakit Mikrovaskular: Pada tingkat mikroskopis, hiperglikemia menyebabkan disfungsi endotel, penebalan membran basal kapiler, dan keadaan pro-trombotik. Perubahan ini semakin mengganggu perfusi di tingkat jaringan, memperburah hipoksia, dan mendorong nekrosis. Gangren adalah manifestasi klinis dari kematian jaringan masif akibat iskemia berat ini.
Gambar 1. Skema patofisiologi diabetic foot
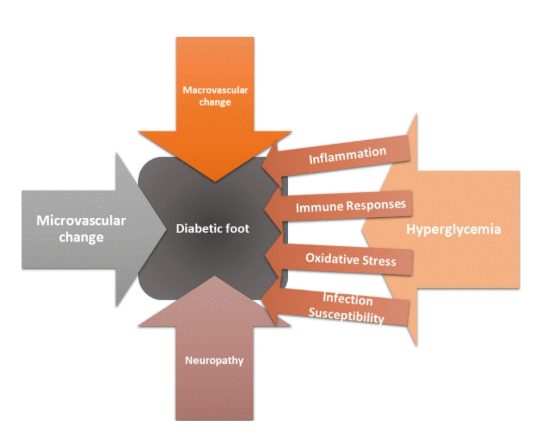
1.3. Kompromi Imunologis: Pertahanan yang Melemah
Hiperglikemia secara langsung menekan fungsi sistem imun bawaan dan adaptif, sebuah kondisi yang dikenal sebagai imunopati diabetik. Pertahanan tubuh yang melemah ini membuat pasien sangat rentan terhadap infeksi invasif begitu sawar kulit rusak. Gangguan ini mencakup fungsi neutrofil yang terganggu (kemotaksis, fagositosis, dan oxidative burst), disregulasi pelepasan sitokin yang menciptakan keadaan pro-inflamasi berkepanjangan yang justru menghambat fase proliferasi dan remodeling penyembuhan luka, serta penurunan fungsi sel imun lainnya.
Akibatnya, invasi bakteri awal yang pada individu sehat dapat diatasi dengan mudah, pada pasien diabetes dapat dengan cepat berkembang menjadi infeksi yang merusak dan tidak terkendali.
Secara kolektif, patofisiologi ini menggambarkan suatu rangkaian kausal yang tak terhindarkan: penyakit sistemik (diabetes) menyebabkan triad kelainan lokal (neuropati, PAD, imunopati), yang kemudian memfasilitasi terjadinya ulserasi akibat trauma minor. Ulkus yang terbentuk pada kaki yang iskemik dan imunokompromais ini menjadi tempat ideal bagi infeksi untuk berkembang biak, yang pada akhirnya berujung pada nekrosis jaringan luas atau gangren.
Pemahaman ini menggarisbawahi kebenaran klinis yang krusial: terapi antibiotik yang diberikan secara terisolasi, tanpa manajemen agresif terhadap neuropati (misalnya, dengan offloading) dan PAD (dengan revaskularisasi), hampir pasti akan gagal.
Kehadiran gangren itu sendiri adalah penanda pengganti (surrogate marker) untuk kegagalan multi-sistem pada tingkat tungkai, menandakan bahwa lingkungan lokal secara metabolik dan imunologis tidak mampu lagi menopang viabilitas jaringan. Kondisi ini tidak dapat diperbaiki hanya dengan antibiotik sistemik dan menuntut intervensi bedah debridemen sebagai prasyarat mutlak untuk menghentikan proses destruktif dan memberikan kesempatan bagi penyembuhan.
Bagian 2: Penilaian Klinis dan Stratifikasi: Landasan Manajemen
Penilaian klinis yang akurat dan stratifikasi keparahan yang tepat adalah langkah paling krusial dalam manajemen infeksi kaki diabetik (IKD). Kerangka kerja yang disediakan oleh International Working Group on the Diabetic Foot (IWGDF) dan Infectious Diseases Society of America (IDSA) berfungsi sebagai alat pengambilan keputusan utama yang memandu setiap aspek penatalaksanaan, mulai dari triase hingga pemilihan terapi.
2.1. Mendiagnosis Infeksi: Lebih dari Sekadar Luka
Langkah pertama adalah membedakan antara ulkus yang terkolonisasi (yang tidak memerlukan antibiotik) dan ulkus yang terinfeksi secara klinis. Diagnosis IKD adalah diagnosis klinis, bukan mikrobiologis. Infeksi didefinisikan oleh adanya minimal dua dari tanda-tanda peradangan klasik berikut :
Bengkak atau indurasi lokal
Kemerahan (eritema) yang meluas >0.5 cm di sekitar luka
Nyeri tekan atau nyeri lokal
Rasa hangat lokal
Adanya sekret purulen (nanah)
Penting untuk ditekankan bahwa ulkus yang tidak menunjukkan tanda-tanda infeksi ini tidak boleh diobati dengan antibiotik, karena praktik ini tidak terbukti mencegah infeksi dan hanya akan mendorong resistensi antibiotik.
2.2. Klasifikasi Keparahan IWGDF/IDSA: Alat Paling Kritis bagi Dokter Umum
Setelah diagnosis infeksi ditegakkan, langkah selanjutnya yang paling penting adalah mengklasifikasikan tingkat keparahannya. Sistem klasifikasi IWGDF/IDSA adalah fondasi untuk semua keputusan manajemen berikutnya.
Infeksi Ringan (Mild): Infeksi superfisial yang hanya melibatkan kulit dan jaringan subkutan. Eritema di sekelilingnya tidak lebih dari 2 cm. Tidak ada tanda-tanda infeksi sistemik. Pasien dalam kondisi ini umumnya dapat dikelola secara rawat jalan dengan antibiotik oral.
Infeksi Sedang (Moderate): Infeksi dengan eritema yang meluas >2 cm, atau melibatkan struktur yang lebih dalam dari kulit/jaringan subkutan (misalnya, abses, osteomielitis, artritis septik, fasitis). Tidak ada tanda-tanda respons inflamasi sistemik (SIRS). Pasien ini sering kali memerlukan rawat inap dan terapi antibiotik intravena awal.
Infeksi Berat (Severe): Infeksi kaki apa pun yang disertai dengan tanda-tanda SIRS, seperti demam (>38°C) atau hipotermia (<36°C), takikardia (>90 denyut/menit), takipnea (>20 napas/menit), atau status mental yang berubah, serta kelainan hitung sel darah putih. Pasien ini berada dalam kondisi darurat medis yang mengancam jiwa dan tungkai, serta memerlukan rawat inap segera dan intervensi bedah darurat.
Dalam konteks gangren, kondisi ini secara definisi melibatkan nekrosis jaringan dalam. Oleh karena itu, kehadiran gangren secara otomatis mengklasifikasikan infeksi sebagai minimal tingkat sedang. Dokter harus secara aktif mencari kriteria infeksi berat (SIRS). Dengan demikian, asumsi dasar untuk setiap pasien yang datang dengan gangren kaki diabetik adalah bahwa mereka menderita infeksi yang mengancam tungkai dan berpotensi mengancam jiwa, yang memerlukan rujukan segera ke rumah sakit untuk penanganan oleh tim spesialis.
Sistem klasifikasi IWGDF/IDSA ini bukan sekadar alat deskriptif, melainkan sebuah algoritma triase dan prognostik yang kuat. Klasifikasi ini secara langsung menentukan tingkat perawatan yang dibutuhkan (rawat jalan vs. rawat inap), rute pemberian antibiotik (oral vs. intravena), dan urgensi konsultasi bedah. Kesalahan dalam mengklasifikasikan infeksi sedang sebagai ringan dapat menyebabkan kegagalan terapi dengan antibiotik oral.
Kesalahan yang lebih fatal adalah mengklasifikasikan infeksi berat sebagai sedang, yang dapat menyebabkan penundaan intervensi bedah dan resusitasi yang dapat berakibat fatal. Oleh karena itu, kemampuan untuk menerapkan klasifikasi ini secara akurat adalah tugas intelektual paling kritis yang dilakukan oleh seorang dokter di lini pertama.
2.3. Alat Diagnostik Tambahan
Meskipun diagnosis bersifat klinis, beberapa pemeriksaan penunjang dapat membantu dalam kasus yang meragukan atau untuk menilai kedalaman infeksi.
Penanda Inflamasi: C-reactive protein (CRP), laju endap darah (LED), dan procalcitonin (PCT) dapat membantu mengkonfirmasi adanya infeksi dalam kasus-kasus yang tidak jelas, meskipun penanda ini tidak spesifik dan dapat meningkat pada kondisi inflamasi lainnya.
Pencitraan: Foto rontgen polos direkomendasikan untuk semua ulkus baru untuk menyingkirkan adanya deformitas tulang, gas di jaringan lunak, atau benda asing. Namun, untuk mendiagnosis osteomielitis yang mendasarinya,
Magnetic Resonance Imaging (MRI) adalah modalitas pencitraan yang paling sensitif dan spesifik.Uji Probe-to-Bone (PTB): Uji sederhana di samping tempat tidur ini melibatkan eksplorasi dasar ulkus dengan probe logam steril. Jika probe dapat menyentuh tulang dengan mudah, uji ini dianggap positif. Pada pasien dengan risiko tinggi IKD, uji PTB positif memiliki nilai prediksi positif yang tinggi untuk osteomielitis.
Bagian 3: Lanskap Mikrobiologis dan Pentingnya Pengambilan Spesimen yang Tepat
Identifikasi patogen penyebab yang akurat adalah kunci untuk terapi antibiotik definitif dan praktik antimicrobial stewardship yang baik. Hal ini bergantung sepenuhnya pada pemahaman tentang mikroorganisme yang mungkin terlibat dan, yang lebih penting, pada teknik pengambilan spesimen yang benar.
3.1. Sifat Polimikrobial pada Infeksi Kronis dan Berat
Profil mikrobiologis IKD bervariasi tergantung pada tingkat keparahan dan durasi infeksi.
Infeksi ringan yang akut pada pasien yang belum pernah menerima antibiotik sebelumnya (antibiotic-naïve) sering kali bersifat monomikrobial. Patogen yang paling umum adalah kokus Gram-positif aerob, terutama Staphylococcus aureus dan Streptococcus spp..
Sebaliknya, infeksi sedang hingga berat, luka kronis, atau infeksi pada pasien yang baru saja menerima terapi antibiotik, biasanya bersifat polimikrobial. Flora campuran ini sering kali mencakup:
Batang Gram-negatif aerob (misalnya, Escherichia coli, Klebsiella spp., Proteus spp.).
Bakteri anaerob obligat (misalnya, Bacteroides spp., Peptostreptococcus spp.), terutama jika terdapat iskemia atau nekrosis/gangren yang signifikan, karena lingkungan hipoksik mendukung pertumbuhan mereka.
Gambar 2. Gas gangrene pada diabetic foot.
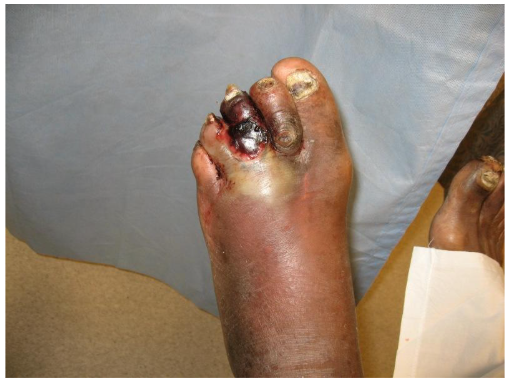
3.2. Standar Emas: Kultur Jaringan Dalam
Pedoman klinis sangat tegas mengenai cara memperoleh spesimen untuk kultur: spesimen harus diambil setelah luka dibersihkan dan didebridemen secara adekuat.
Metode yang Tidak Dianjurkan: Usapan luka superfisial (superficial wound swabs) sangat tidak direkomendasikan. Spesimen semacam ini hampir pasti akan menumbuhkan bakteri komensal atau kolonisator dari permukaan kulit, yang belum tentu merupakan patogen penyebab infeksi invasif di jaringan yang lebih dalam. Hasil kultur dari usapan superfisial dapat menyesatkan klinisi untuk memberikan antibiotik spektrum luas yang tidak perlu, yang berkontribusi pada peningkatan resistensi.
Metode yang Direkomendasikan: Standar emas untuk kultur adalah spesimen jaringan dalam. Ini dapat diperoleh melalui beberapa metode :
Biopsi jaringan: Pengambilan sepotong kecil jaringan dari dasar ulkus yang telah didebridemen.
Kuretase ulkus: Mengerok dasar ulkus dengan kuret untuk mendapatkan jaringan.
Aspirasi: Aspirasi cairan atau pus dari abses atau koleksi cairan yang belum pecah.
Untuk kasus yang dicurigai osteomielitis, biopsi tulang adalah metode diagnostik definitif, baik untuk konfirmasi histologis maupun identifikasi patogen penyebab.
Pilihan metode pengambilan spesimen merupakan penentu kritis dari antimicrobial stewardship. Sampel yang buruk (usapan superfisial) menghasilkan data yang buruk (organisme kolonisator), yang mengarah pada keputusan yang buruk (penggunaan antibiotik spektrum ultra-luas yang tidak perlu) dan mendorong resistensi.
Sebagai contoh, usapan dari permukaan kaki yang gangren hampir pasti akan menumbuhkan berbagai mikroorganisme, termasuk patogen resisten seperti Pseudomonas atau MRSA, yang mungkin hanya berkolonisasi di jaringan nekrotik.
Laporan kultur semacam itu dapat mendorong klinisi untuk memberikan terapi yang sangat luas, seperti kombinasi karbapenem dan vankomisin. Namun, patogen yang sebenarnya menyerang jaringan dalam mungkin adalah organisme yang lebih rentan.
Dengan memperoleh kultur jaringan dalam yang tepat setelah debridemen, klinisi dapat mengidentifikasi patogen invasif yang sebenarnya, yang memungkinkan de-eskalasi ke antibiotik yang lebih sempit dan bertarget setelah hasil sensitivitas tersedia. Bagi dokter umum, implikasi praktisnya adalah bahwa dalam konteks gangren yang memerlukan debridemen bedah, kultur yang paling berharga adalah yang diambil secara intraoperatif oleh ahli bedah.
Peran dokter umum adalah memulai terapi empiris spektrum luas dan memahami bahwa terapi ini akan disesuaikan berdasarkan spesimen berkualitas tinggi yang diperoleh selama intervensi bedah yang diperlukan. Oleh karena itu, rujukan tidak boleh ditunda hanya untuk mendapatkan kultur superfisial yang nilainya terbatas.
Bagian 4: Terapi Antibiotik Empiris: Regimen Berbasis Bukti untuk Dokter Umum
Bagian ini menyajikan inti praktis dari manajemen farmakologis, memberikan rekomendasi antibiotik yang jelas dan bertingkat berdasarkan keparahan infeksi. Ini secara langsung menjawab kebutuhan akan informasi tentang "Antibiotik Gangren Pedis" dan "Dosis Obat Gangren Pedis" dengan pendekatan berbasis bukti.
4.1. Prinsip Ekuivalensi: Peluang untuk Stewardship
Sebuah temuan krusial dari berbagai tinjauan sistematis dan meta-analisis adalah bahwa untuk IKD tingkat sedang hingga berat, banyak regimen antibiotik spektrum luas yang direkomendasikan memiliki efikasi klinis yang sebanding. Sebagai contoh, studi menunjukkan tidak ada perbedaan signifikan dalam resolusi klinis antara piperacillin-tazobactam dan ertapenem , atau antara fluoroquinolon dan piperacillin-tazobactam.
Sebaliknya, tigecycline tercatat kurang efektif dibandingkan ertapenem dan memiliki lebih banyak efek samping, sehingga tidak direkomendasikan sebagai pilihan utama.
Temuan ekuivalensi ini merupakan mandat untuk antimicrobial stewardship. Antibiotik "terbaik" bukanlah yang memiliki spektrum terluas, melainkan yang efektif, aman, sesempit mungkin, dan disesuaikan dengan data epidemiologi lokal serta faktor pasien. Ini menentang heuristik klinis umum untuk "menggunakan senjata pamungkas" (misalnya, karbapenem) untuk semua infeksi berat.
Seorang dokter umum di lingkungan dengan tingkat resistensi rendah dapat secara tepat menggunakan ampicillin-sulbactam atau kombinasi ceftriaxone plus metronidazole, yang sama berbasis buktinya dengan penggunaan karbapenem yang lebih mahal, sehingga dapat menyimpan karbapenem untuk infeksi yang benar-benar resisten.
4.2. Regimen Berdasarkan Tingkat Keparahan
Pilihan antibiotik empiris harus didasarkan pada klasifikasi keparahan IWGDF/IDSA.
Infeksi Ringan: Terapi dapat diberikan secara oral dan ditargetkan pada kokus Gram-positif. Pilihan yang sesuai termasuk sefaleksin, amoksisilin-klavulanat, doksisiklin, atau klindamisin.
Infeksi Sedang: Memerlukan cakupan yang lebih luas untuk kokus Gram-positif, batang Gram-negatif, dan sering kali anaerob. Pengobatan harus dimulai dengan terapi intravena (IV), dengan kemungkinan peralihan ke agen oral dengan bioavailabilitas tinggi setelah ada perbaikan klinis yang jelas. Pilihan IV termasuk ampicillin-sulbactam, piperacillin-tazobactam, atau karbapenem (ertapenem, imipenem). Kombinasi seperti ceftriaxone plus metronidazole juga merupakan alternatif yang valid. Pilihan peralihan oral (step-down) termasuk moksifloksasin atau levofloksasin plus klindamisin.
Infeksi Berat: Selalu memerlukan terapi parenteral spektrum luas awal yang mencakup kokus Gram-positif, batang Gram-negatif, dan anaerob. Ini adalah keadaan darurat yang memerlukan rawat inap. Regimennya serupa dengan infeksi sedang tetapi selalu dimulai secara IV dan sering kali dengan dosis yang lebih agresif. Kandidat utama adalah piperacillin-tazobactam atau karbapenem (imipenem-cilastatin, meropenem), dengan atau tanpa penambahan vankomisin tergantung pada faktor risiko MRSA.
4.3. Dosis Obat, Rute, dan Durasi
Durasi: Untuk infeksi jaringan lunak, durasi terapi 1 hingga 2 minggu biasanya sudah cukup. Durasi ini dapat diperpanjang hingga 3 atau 4 minggu jika infeksi membaik tetapi resolusinya lebih lambat dari yang diharapkan atau jika pasien memiliki PAD yang parah. Durasi yang direkomendasikan ini sering kali lebih pendek dari praktik tradisional dan merupakan perubahan berbasis bukti penting yang perlu diadopsi untuk mengurangi paparan antibiotik yang tidak perlu. Fokusnya adalah pada resolusi tanda-tanda klinis infeksi, bukan pada penyembuhan luka sepenuhnya, yang bisa memakan waktu lebih lama. Osteomielitis memerlukan durasi yang jauh lebih lama, sering kali 6 minggu atau lebih setelah debridemen yang adekuat.
Rute: Infeksi ringan diobati secara oral. Infeksi sedang hingga berat dimulai dengan terapi IV, dengan peralihan ke terapi oral dipandu oleh perbaikan klinis dan ketersediaan agen oral dengan bioavailabilitas tinggi.
Tabel berikut merangkum rekomendasi ini menjadi alat klinis praktis.
Tabel 1: Rekomendasi Antibiotik Empiris dan Dosis Obat untuk Infeksi Kaki Diabetik dengan Gangren (berdasarkan Klasifikasi IWGDF/IDSA)
Tingkat Keparahan Infeksi (IWGDF/IDSA) | Kemungkinan Patogen Utama | Regimen Pilihan Utama (Parenteral/IV) | Dosis Obat dan Frekuensi (Dewasa dengan Fungsi Ginjal Normal) | Regimen Alternatif atau Oral Step-Down | Dosis Obat dan Frekuensi (Oral) | Durasi Terapi (Jaringan Lunak) | Pertimbangan Klinis Penting |
Ringan | Staphylococcus aureus, Streptococcus spp. | Tidak diindikasikan (terapi oral) | N/A | Amoksisilin-klavulanat | 875 mg/125 mg setiap 12 jam | 1-2 minggu | Pertimbangkan doksisiklin atau TMP-SMX jika ada risiko MRSA. |
Sefaleksin | 500 mg setiap 6 jam | ||||||
Klindamisin | 300-450 mg setiap 8 jam | ||||||
Sedang | Polimikrobial: Kokus Gram-positif, Batang Gram-negatif, Anaerob | Ampicillin-sulbactam | 3 g IV setiap 6 jam | Moksifloksasin | 400 mg setiap 24 jam | 1-3 minggu | Mulai dengan IV, pertimbangkan step-down ke oral setelah stabilisasi klinis. Ertapenem tidak mencakup Pseudomonas. |
Piperacillin-tazobactam | 3.375 g IV setiap 6 jam atau 4.5 g IV setiap 8 jam | Levofloksasin + Klindamisin | 750 mg setiap 24 jam + 300-450 mg setiap 8 jam | Penyesuaian dosis diperlukan pada gangguan ginjal. | |||
Ertapenem | 1 g IV setiap 24 jam | Amoksisilin-klavulanat | 875 mg/125 mg setiap 12 jam | ||||
Ceftriaxone + Metronidazole | 1-2 g IV setiap 24 jam + 500 mg IV setiap 8 jam | ||||||
Berat (dengan/tanpa SIRS) | Polimikrobial: Kokus Gram-positif, Batang Gram-negatif, Anaerob, kemungkinan patogen resisten | Piperacillin-tazobactam | 4.5 g IV setiap 6 jam | Terapi IV dilanjutkan hingga perbaikan signifikan; step-down oral dilakukan dengan hati-hati. | N/A untuk fase akut | 2-4 minggu | Selalu rawat inap. Pertimbangkan penambahan Vankomisin atau Linezolid jika ada risiko tinggi MRSA. Regimen harus mencakup Pseudomonas (misalnya, Pip-Tazo, Meropenem). |
Imipenem-cilastatin | 500 mg IV setiap 6 jam | Memerlukan konsultasi bedah dan penyakit infeksi segera. | |||||
Meropenem | 1 g IV setiap 8 jam | Pantau fungsi ginjal dengan cermat. | |||||
+ Vankomisin (jika ada risiko MRSA) | 15-20 mg/kg IV setiap 8-12 jam (sesuaikan dengan kadar) |
Bagian 5: Menavigasi Patogen Resisten: MRSA dan Pseudomonas aeruginosa
Manajemen IKD yang modern menuntut pendekatan yang bijaksana terhadap kemungkinan adanya patogen resisten. Keputusan untuk memberikan cakupan empiris terhadap Methicillin-Resistant Staphylococcus aureus (MRSA) dan Pseudomonas aeruginosa harus didasarkan pada penilaian risiko yang cermat, bukan sebagai tindakan rutin, untuk menjaga efektivitas antibiotik dan meminimalkan efek samping.
5.1. Methicillin-Resistant Staphylococcus aureus (MRSA)
Cakupan empiris untuk MRSA tidak diperlukan secara rutin pada IKD ringan hingga sedang. Pemberian antibiotik anti-MRSA yang tidak perlu hanya akan meningkatkan biaya, risiko efek samping, dan tekanan resistensi. Namun, cakupan ini harus dipertimbangkan secara serius pada pasien dengan faktor risiko spesifik berikut :
Riwayat infeksi atau kolonisasi MRSA sebelumnya.
Rawat inap atau penggunaan antibiotik dalam beberapa bulan terakhir.
Prevalensi MRSA yang tinggi di komunitas atau institusi lokal.
Infeksi yang berat dan mengancam tungkai, di mana kegagalan terapi awal dapat berakibat fatal.
Pilihan Terapi: Jika MRSA dicurigai, agen yang sesuai harus ditambahkan ke regimen spektrum luas.
Untuk infeksi sedang hingga berat (IV): Vankomisin adalah pilihan utama. Linezolid (tersedia IV dan oral) dan daptomisin adalah alternatif yang efektif. Linezolid memiliki bioavailabilitas oral 100% yang sangat baik, menjadikannya pilihan step-down yang menarik, tetapi dikaitkan dengan risiko toksisitas hematologis (trombositopenia) dan neuropati pada penggunaan jangka panjang, serta interaksi obat (sindrom serotonin).
Untuk infeksi ringan (Oral): Doksisiklin atau trimetoprim-sulfametoksazol (TMP-SMX) dapat menjadi pilihan yang efektif untuk strain MRSA yang didapat dari komunitas (community-acquired).
5.2. Pseudomonas aeruginosa
Serupa dengan MRSA, cakupan empiris rutin untuk P. aeruginosa umumnya tidak diperlukan pada IKD ringan hingga sedang di iklim sedang. Namun, patogen ini harus dicurigai dan dicakup dalam skenario klinis tertentu:
Infeksi berat.
Paparan air yang signifikan pada kaki (misalnya, berendam, kolam renang).
Pasien yang tinggal di iklim hangat atau tropis (seperti Indonesia), di mana Pseudomonas lebih umum ditemukan di lingkungan.
Jika P. aeruginosa telah diisolasi dari kultur di lokasi yang sama pada beberapa minggu sebelumnya.
Pilihan Terapi: Jika Pseudomonas menjadi perhatian, antibiotik beta-laktam yang dipilih harus memiliki aktivitas anti-pseudomonal.
Pilihan utama termasuk piperacillin-tazobactam, ceftazidime (sefalosporin generasi ketiga), cefepime (sefalosporin generasi keempat), atau karbapenem seperti imipenem atau meropenem.
Penting untuk dicatat bahwa ertapenem, meskipun merupakan karbapenem, tidak memiliki aktivitas yang andal terhadap P. aeruginosa dan tidak boleh digunakan jika patogen ini dicurigai.
Fluoroquinolon seperti siprofloksasin atau levofloksasin juga memiliki aktivitas anti-pseudomonal dan dapat menjadi bagian dari regimen kombinasi atau sebagai pilihan oral step-down.
Keputusan untuk memberikan cakupan empiris terhadap MRSA atau Pseudomonas adalah sebuah kalkulasi risiko-manfaat. Pendekatan ini mewakili pergeseran dari paradigma lama "cakup semuanya" ke pendekatan modern "cakup apa yang paling mungkin berdasarkan konteks pasien dan epidemiologi lokal."
Bagi dokter umum, ini berarti melakukan anamnesis yang lebih rinci mengenai riwayat rawat inap, penggunaan antibiotik, hasil kultur sebelumnya, dan faktor lingkungan adalah kegiatan yang sangat bernilai. Misalnya, memilih piperacillin-tazobactam daripada ertapenem adalah pilihan yang disengaja yang dibuat hanya ketika risiko Pseudomonas tinggi; jika tidak, ertapenem dengan spektrum yang lebih sempit mungkin lebih disukai untuk meminimalkan kerusakan kolateral pada mikrobioma pasien.
Bagian 6: Peran Mutlak Intervensi Bedah dan Terapi Adjuvan
Dalam penatalaksanaan gangren kaki diabetik, antibiotik memainkan peran pendukung yang penting, tetapi bukan peran utama. Terapi definitif untuk jaringan nekrotik dan infeksi dalam adalah intervensi bedah. Mengandalkan antibiotik saja dalam menghadapi jaringan mati adalah resep untuk kegagalan, yang akan berujung pada infeksi yang tidak terkontrol dan amputasi yang lebih tinggi.
6.1. Pembedahan: Terapi Definitif untuk Kontrol Sumber Infeksi
Antibiotik sering kali tidak cukup tanpa intervensi bedah yang tepat untuk mengontrol sumber infeksi (source control). Konsultasi bedah darurat adalah
wajib untuk semua infeksi berat dan infeksi sedang yang disertai komplikasi seperti abses dalam, gangren atau nekrosis yang luas, atau sindrom kompartemen. Gangren, per definisinya, adalah jaringan mati yang tidak memiliki suplai darah, sehingga tidak dapat dijangkau oleh antibiotik sistemik dan tidak dapat hidup kembali. Jaringan ini berfungsi sebagai medium yang subur untuk pertumbuhan bakteri dan harus dihilangkan secara fisik.
Tujuan intervensi bedah meliputi :
Insisi dan drainase: Untuk mengeluarkan pus dari abses.
Debridemen ekstensif: Pengangkatan semua jaringan nekrotik, terinfeksi, dan non-viabel hingga mencapai jaringan sehat yang berdarah. Ini adalah langkah paling kritis untuk menghentikan penyebaran infeksi.
Reseksi tulang: Untuk osteomielitis, tulang yang terinfeksi harus diangkat.
Amputasi: Jika infeksi terlalu luas dan tidak dapat diselamatkan, amputasi (misalnya, jari kaki, transmetatarsal, atau di bawah lutut) diperlukan untuk menyelamatkan sisa tungkai dan, dalam kasus infeksi berat, nyawa pasien.
6.2. Imperatif Vaskular
Kehadiran gangren menandakan iskemia kritis dan menuntut penilaian vaskular yang mendesak oleh spesialis vaskular. Revaskularisasi, baik melalui angioplasti, stenting, atau bedah bypass, sering kali menjadi prasyarat untuk penyembuhan luka dan untuk mencegah kehilangan jaringan lebih lanjut. Tanpa aliran darah yang memadai, tidak ada penyembuhan yang dapat terjadi, dan antibiotik tidak akan pernah mencapai targetnya dalam konsentrasi terapeutik.
6.3. Terapi Adjuvan dan Perawatan Luka
Meskipun antibiotik dan pembedahan adalah pilar utama, pendekatan holistik sangat penting.
Offloading: Mutlak diperlukan untuk menyembuhkan ulkus apa pun di area penahan beban. Ini dapat dicapai dengan total contact cast (TCC), removable cast walker, atau alas kaki terapeutik.
Perawatan Luka: Setelah debridemen, menjaga lingkungan luka yang lembab dengan pembalut yang sesuai sangat penting untuk mendukung proses penyembuhan.
Terapi Adjuvan: Peran terapi tambahan masih terus dievaluasi. Terapi oksigen hiperbarik (HBOT) dan granulocyte colony-stimulating factors (G-CSF) dapat membantu mencegah amputasi pada beberapa pasien yang tidak merespons terapi standar, tetapi ini bukan pengganti untuk perawatan standar. Semen tulang yang mengandung antibiotik (
antibiotic-laden bone cement) adalah pilihan yang muncul untuk mengatasi defek tulang yang terinfeksi setelah reseksi.
Bagi dokter umum, paradigma penanganan IKD sedang hingga berat dengan gangren harus bergeser dari "mengobati" menjadi "mendiagnosis, menstabilkan, dan merujuk." Peran utamanya adalah sebagai seorang diagnostisi yang ahli dan fasilitator rujukan bedah darurat. Istilah "pengobatan antibiotik" dalam konteks gangren sebenarnya kurang tepat; istilah yang lebih akurat adalah "terapi antibiotik adjuvan." Kerangka berpikir ini membantu memperjelas prioritas: pisau bedah adalah "pengobatan" utama untuk jaringan nekrotik, sedangkan antibiotik adalah "adjuvan" untuk mengobati selulitis di sekitarnya dan mencegah penyebaran sistemik.
Bagian 7: Kesimpulan: Strategi Multidisiplin untuk Penyelamatan Tungkai
Manajemen gangren kaki diabetik adalah salah satu tantangan paling kompleks dalam kedokteran klinis, yang membutuhkan perpaduan antara penilaian cepat, farmakoterapi berbasis bukti, intervensi bedah yang agresif, dan perawatan terkoordinasi jangka panjang. Keberhasilan dalam menyelamatkan tungkai dan nyawa pasien tidak bergantung pada satu intervensi tunggal, melainkan pada eksekusi yang mulus dari serangkaian tindakan oleh tim multidisiplin.
7.1. Poin Aksi Kunci untuk Dokter Umum
Dokter umum berada di garda terdepan dan memegang peran krusial sebagai penjaga gerbang dan inisiator seluruh alur perawatan. Tindakan awal mereka memiliki dampak yang mendalam pada hasil akhir pasien. Alur kerja kritis untuk dokter umum dapat diringkas menjadi empat langkah:
Kenali (Recognize): Identifikasi tanda-tanda klinis infeksi berdasarkan kriteria IWGDF/IDSA. Bedakan antara ulkus terkolonisasi dan terinfeksi.
Klasifikasikan (Classify): Gunakan sistem klasifikasi IWGDF/IDSA untuk menentukan tingkat keparahan (Ringan, Sedang, Berat). Ini adalah langkah pengambilan keputusan yang paling penting.
Bertindak (Act): Mulai terapi antibiotik empiris yang sesuai dengan tingkat keparahan yang telah ditentukan, dengan mempertimbangkan faktor risiko pasien dan data epidemiologi lokal.
Rujuk (Refer): Untuk setiap infeksi yang diklasifikasikan sebagai sedang atau berat, terutama jika disertai gangren, lakukan rujukan segera ke rumah sakit yang memiliki tim perawatan kaki diabetik multidisiplin.
7.2. Tim Multidisiplin: Standar Perawatan
Bukti secara konsisten menunjukkan bahwa manajemen yang berhasil dan penyelamatan tungkai secara signifikan lebih baik ketika ditangani oleh tim perawatan kaki yang terkoordinasi dan multidisiplin. Tim ideal ini harus mencakup keahlian dari berbagai bidang, termasuk:
Spesialis Bedah (Bedah Vaskular, Bedah Ortopedi, atau Bedah Umum dengan minat khusus)
Spesialis Penyakit Infeksi
Endokrinolog/Diabetolog
Podiatris atau ahli perawatan kaki
Perawat spesialis luka
Spesialis Radiologi Intervensi
Kolaborasi yang erat di antara para spesialis ini memungkinkan pengambilan keputusan yang komprehensif dan terintegrasi, mulai dari optimalisasi kontrol glikemik dan revaskularisasi hingga debridemen bedah dan terapi antibiotik yang ditargetkan.
7.3. Kata Akhir: Dari Resep ke Kemitraan
Pada akhirnya, penatalaksanaan gangren kaki diabetik menuntut pergeseran pola pikir bagi dokter umum—dari seorang pemberi resep independen menjadi mitra lini pertama yang vital dalam jalur perawatan multi-spesialis yang kompleks. Pengenalan yang cepat, stratifikasi yang akurat, dan rujukan yang tangkas adalah kunci untuk meningkatkan hasil akhir pasien, mengurangi angka amputasi, dan meringankan beban besar yang ditimbulkan oleh komplikasi diabetes yang menghancurkan ini.
Referensi
[Physiopathology of the diabetic foot] - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/18822248/
Pathophysiology and Principles of Management of the Diabetic Foot - Mechanisms of Vascular Disease - NCBI Bookshelf, diakses Juli 21, 2025, https://www.ncbi.nlm.nih.gov/books/NBK534268/
A Review of the Pathophysiology, Classification, and Treatment of Foot Ulcers in Diabetic Patients, diakses Juli 21, 2025, https://diabetesjournals.org/clinical/article/27/2/52/85/A-Review-of-the-Pathophysiology-Classification-and
Diabetic foot ulcer: A comprehensive review of pathophysiology and management modalities - PMC, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10037283/
Investigating Diabetic Foot Pathophysiology and Amputation Prevention Strategies through Behavioral Modification, diakses Juli 21, 2025, https://www.jwmr.org/m/journal/view.php?number=459
Understanding the multifaceted etiopathogenesis of foot complications in individuals with diabetes - PMC, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10037285/
Diabetic Foot Infections - StatPearls - NCBI Bookshelf, diakses Juli 21, 2025, https://www.ncbi.nlm.nih.gov/books/NBK441914/
Diabetic Foot Ulcers: Pathophysiology, Immune Dysregulation, and Emerging Therapeutic Strategies - MDPI, diakses Juli 21, 2025, https://www.mdpi.com/2227-9059/13/5/1076
The pathophysiology of diabetic foot: a narrative review, diakses Juli 21, 2025, https://www.e-jyms.org/journal/view.php?number=2810
The pathophysiology of diabetic foot: a narrative review - PMC - PubMed Central, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10626291/
IWGDF/IDSA Guidelines on the Diagnosis and Treatment of Diabetes-related Foot Infections ... - Oxford Academic, diakses Juli 21, 2025, https://academic.oup.com/cid/advance-article/doi/10.1093/cid/ciad527/7287196
2012 Infectious Diseases Society of America Clinical Practice Guideline for the Diagnosis and Treatment of Diabetic Foot Infectionsa - Oxford Academic, diakses Juli 21, 2025, https://academic.oup.com/cid/article/54/12/e132/455959
2012 Infectious Diseases Society of America clinical practice guideline for the diagnosis and treatment of diabetic foot infections - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/22619242/
Diagnosis and treatment of diabetic foot infections - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/16799390/
New international guidelines tackle diabetic foot infection diagnosis, treatment, diakses Juli 21, 2025, https://diabetes.acponline.org/archives/2023/10/13/1.htm
Diabetes-Related Foot Infections: Institutional Treatment Guidance, diakses Juli 21, 2025, https://www.unmc.edu/intmed/_documents/id/asp/clinicalpath-dfi_institutional_guideline_final.pdf
Diabetic Foot Ulcers - Foot & Ankle - Orthobullets, diakses Juli 21, 2025, https://www.orthobullets.com/foot-and-ankle/7046/diabetic-foot-ulcers
A systematic review and meta-analysis of randomized controlled trials of systemic antibiotics for diabetes-related foot infections, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/pmid/39931793/
Guidelines on the diagnosis and treatment of foot infection in persons with diabetes (IWGDF 2019 update), diakses Juli 21, 2025, https://iwgdfguidelines.org/wp-content/uploads/2020/11/Lipsky_et_al-2020-IWGDF-infection-guideline.pdf
IWGDF Guideline on the diagnosis and treatment of foot infection in persons with diabetes, diakses Juli 21, 2025, https://iwgdfguidelines.org/wp-content/uploads/2019/05/05-IWGDF-infection-guideline-2019.pdf
Systemic antibiotics for treating diabetic foot infections - PMC - PubMed Central, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC8504988/
A Systematic Review of Randomized Controlled Trials of Antibiotic Use in Diabetic Foot Ulcer Infections: Focus on Clinical Cure - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/35384424/
Systemic Antimicrobial Therapy for Diabetic Foot Infections: An ..., diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC10295044/
Antibiotic therapy of diabetic foot infections: A systematic review of randomized controlled trials - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/30099812/
The treatment of diabetic foot infections: focus on ertapenem - PMC - PubMed Central, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC2788600/
Diabetes-Related Foot Infections: Diagnosis and Treatment - AAFP, diakses Juli 21, 2025, https://www.aafp.org/pubs/afp/issues/2021/1000/p386.html
A systematic review and meta-analysis of randomized controlled trials of systemic antibiotics for diabetes-related foot infections - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/39931793/
Guidelines on offloading foot ulcers in persons with diabetes (IWGDF 2023 update), diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/37226568/
Diabetic foot infections: stepwise medical and surgical management - PMC, diakses Juli 21, 2025, https://pmc.ncbi.nlm.nih.gov/articles/PMC7951343/
Antibiotic-laden bone cement for diabetic foot infected wounds: A systematic review and meta-analysis - PubMed, diakses Juli 21, 2025, https://pubmed.ncbi.nlm.nih.gov/37008902/
IWGDF Guidelines on the prevention and management of diabetes ..., diakses Juli 21, 2025, https://iwgdfguidelines.org/wp-content/uploads/2023/07/IWGDF-Guidelines-2023.pdf